中国苏州,2026年5月11日——基石药业(股票代码:2616.HK),一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,今日宣布其高选择性RET抑制剂普拉替尼胶囊(100 mg)的首批地产化产品已完成生产及放行,并正式启动全国商业化发货。这标志着该创新药的国内供应链自主化迈出关键一步。
普拉替尼胶囊首批地产化产品发货现场

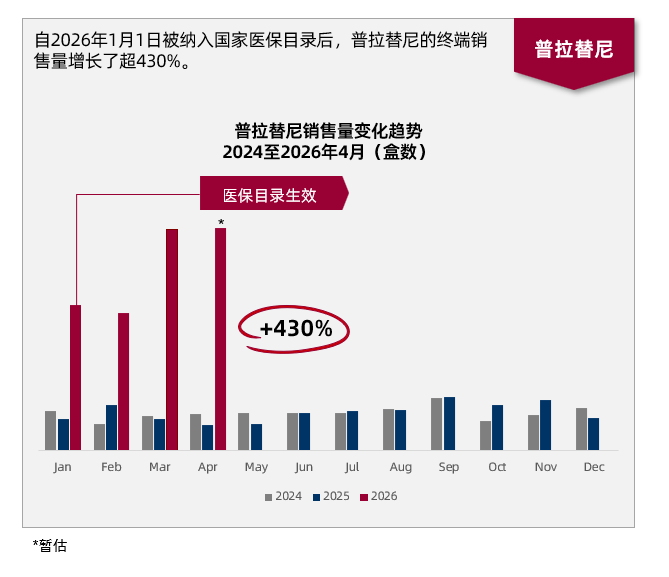
普拉替尼胶囊于2025年底首次获纳入《国家基本医疗保险、生育保险和工伤保险药品目录》(“国家医保目录”),并自2026年1月1日起生效。受益于国家医保目录准入对患者可及性的显著提升,截至2026年4月,普拉替尼胶囊的终端销售量较去年同期快速增长超430%。基于这一增长趋势,预计2026年全年普拉替尼胶囊销售收入有望超过人民币3亿元。
普拉替尼胶囊终端销售量同比增长超430%
基石药业首席执行官、研发总裁及执行董事杨建新博士表示:“首批地产化普拉替尼胶囊的顺利发货,是我们生产、质量、注册及供应链等团队严格遵循国际标准、高效协同的成果。通过严谨的技术转移与工艺验证,我们确保了地产化产品与进口产品在质量和疗效上高度可比。随着本土化生产及供应体系的成熟,我们将充分承接国家医保目录落地后释放的临床需求,切实保障药品的可及性与供应稳定性。同时,全链条的本地化将显著优化我们的成本结构,提升盈利韧性与商业化活力。展望未来,基石药业将继续坚守初心,确保高质量药物的稳定供应,惠及更多中国患者。”
关于普拉替尼胶囊
普拉替尼胶囊是一种口服、每日一次、强效高选择性RET抑制剂。已获中国国家药监局(NMPA)批准用于一线治疗局部晚期或转移性RET融合阳性非小细胞肺癌(NSCLC)成人患者,治疗先前经含铂化疗后的局部晚期或转移性RET融合阳性NSCLC的成人患者;及RET融合阳性甲状腺癌(TC)患者。此外,该药物获香港卫生署批准用于治疗局部晚期或转移性RET融合阳性NSCLC患者,并获台湾食品药物管理署(TFDA)批准用于治疗局部晚期或转移性RET融合阳性NSCLC及晚期或转移性RET融合阳性TC成年患者。
美国食品药品监督管理局(FDA)批准其以商品名为GAVRETO®上市销售,适应症分别为:
*甲状腺癌适应症基于客观缓解率(ORR)和缓解持续时间(DOR)数据在加速审批途径下获得批准。针对该适应症的常规批准可能取决于确证性试验中临床获益的验证和描述。
普拉替尼胶囊由基石药业合作伙伴Blueprint Medicines公司(已于2025年7月被赛诺菲收购)开发。基石药业拥有普拉替尼胶囊在大中华地区(包括中国大陆、中国香港、中国澳门和中国台湾地区)的独家开发和商业化权利。2023年11月,基石药业将普拉替尼胶囊在中国大陆区域的独家商业化推广权授予上海艾力斯医药科技股份有限公司。
关于基石药业
基石药业(香港联交所代码: 2616)成立于2015年底,是一家专注于肿瘤、免疫与炎症等关键疾病领域药物研发的创新驱动型生物医药企业,致力于满足中国和全球患者的殷切医疗需求。截至目前,公司已成功上市4款创新药、获批21项新药上市申请(NDA)以及9项适应症。当前研发管线均衡配置了抗体偶联药物(ADC)、多特异性抗体、以及免疫疗法和精准治疗药物在内的16款候选药物。同时,基石药业拥有一支资深管理团队,“全链条”覆盖临床前探索、临床转化、临床开发、药物生产、商务拓展、商业运营等关键环节。如需了解有关基石药业的更多信息,请访问:www.cstonepharma.com。
投资者关系: ir@cstonepharma.com
媒体关系:pr@cstonepharma.com
前瞻性声明
本文所作出的前瞻性陈述仅与本文作出该陈述当日的事件或资料有关。除法律规定外,于作出前瞻性陈述当日之后,无论是否出现新资料、未来事件或其他情况,我们并无责任更新或公开修改任何前瞻性陈述及预料之外的事件。请细阅本文,并理解我们的实际未来业绩或表现可能与预期有重大差异。本文内所有陈述乃本文章刊发日期作出,可能因未来发展而出现变动。
声明:仅供医疗卫生专业人士交流使用。
Blueprint Medicines及其相关商标为Blueprint Medicines公司所有。GAVRETO®及其相关商标在美国以外地区为Blueprint Medicines公司所有。